INVESTIGACIÓN: FUERZAS INTERMOLECULARES , INTERACCIONES DIPOLO-DIPOLO EINTERACCIONES PUENTES DE HIDRÓGENO
FUERZAS
INTERMOLECULARES
Las fuerzas intermoleculares se
definen como el conjunto de fuerzas atractivas y repulsivas que se producen
entre las moléculas como consecuencia de la polaridad que poseen las moléculas.
Cuando dos o más átomos se unen mediante un enlace químico forman
una molécula, los electrones que conforman la nueva molécula recorren y se
concentran en la zona del átomo con mayor electronegatividad, definimos la
electronegatividad como la propiedad que tienen los átomos en atraer
electrones. La concentración de los electrones en una zona definida de la
molécula crea una carga negativa, mientras que la ausencia de los electrones
crea una carga positiva.
Denominamos dipolos a las moléculas que disponen de zonas cargadas
negativamente y positivamente debido a la electronegatividad y concentración de
los electrones en las moléculas.
Podemos asimilar el funcionamiento de un dipolo a
un imán con su polo positivo y su polo negativo, de tal forma que si acercamos
otro imán el polo positivo atraerá al polo negativo y viceversa, dando como
resultado una unión.

FUERZAS
INTERMOLECULARES 2
Las
fuerzas atractivas entre moléculas, las llamadas fuerzas intermoleculares,
son las responsables del comportamiento no ideal de los gases. Ellas juegan un
papel importante también en los distintos estados de agregación de la materia
(líquido, sólido o gas).
Generalmente,
las fuerzas intermoleculares son mucho más débiles que las intramoleculares.
Así, por ejemplo, se requiere menos energía para evaporar un líquido que para
romper los enlaces de las moléculas de dicho líquido. Para entender las
propiedades de los distintos estados de la materia, necesitamos comprender y
conocer los distintos tipos de fuerzas intermoleculares.

Los
átomos de una molécula se mantienen unidos por enlaces químicos cuya fuerza va
de 150 a 1000 kJ/mol. Otras fuerzas de atracción más débiles, llamadas
fuerzas intermoleculares o atracciones intermoleculares,
atraen una molécula a otra. Por ejemplo, se requieren 1652 kJ para romper 4
moles de enlaces covalentes C¾H y separar el átomo de C y los cuatro átomos de
H de todas las moléculas de 1 mol de metano:
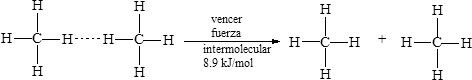
Pero
sólo se requieren 8.9 kJ para separar unas de otras 1 mol de moléculas de
metano que están muy juntas en el metano líquido, a fin de evaporar el líquido
y convertirlo en gaseoso.
Las
atracciones moleculares son más débiles que los enlaces covalentes porque no
son el resultado de compartir pares de electrones entre átomos; es decir, son
interacciones no covalentes: fuerzas de atracción que no son enlaces
iónicos y que son diferentes de los enlaces covalentes. Las interacciones no
covalentes entre moléculas (fuerzas intermoleculares) explican el
punto de fusión, el punto de ebullición y otras propiedades de las sustancias
que no son iónicas. Las interacciones no covalentes entre diferentes partes de
una molécula grande (fuerzas intramoleculares) mantienen las
moléculas de importancia biológica con la forma exacta que requieren para
desempeñar sus funciones. Por ejemplo, un gran número de interacciones no
covalentes entre las cadenas de ADN establecen la estructura de doble hélice de
esta molécula de gran tamaño. Sin embargo, las interacciones no covalentes
individuales dentro del ADN son bastante débiles como para que sean vencidas en
condiciones fisiológicas, lo cual hace posible la separación de las dos cadenas
del ADN para copiarlos.
En
las siguientes secciones exploraremos estos tipos de interacciones no
covalentes, conocidas en conjunto como fuerzas de van der Waals (fuerzas de
London, atracciones dipolo-dipolo) y puentes de hidrógeno. Estas fuerzas son
las que contribuyen al término n2a/V2 en la ecuación
de van der Waals para los gases no ideales.
INTERACCIONES
DIPOLO-DIPOLO
Interacción entre los dipolos eléctricos de las moléculas de cloruro de hidrógeno.
La interacción dipolo-dipolo consiste en la atracción electrostática entre
el extremo positivo de una molécula polar y el negativo de otra. El enlace de hidrógeno es un tipo
especial de interacción dipolo-dipolo.
Las fuerzas electrostáticas entre dos iones disminuyen de acuerdo con un
factor 1/d2 a medida que aumenta su separación d.
En cambio, las fuerzas dipolo dipolo varían según 1/d3 (d elevado
a la tercera potencia) y sólo son eficaces a distancias muy
cortas; además son fuerzas más débiles que en el caso ion-ion porque q+ y q-
representan cargas parciales. Las energías promedio
de las interacciones dipolo dipolo son aproximadamente 4 kJ pormol, en contraste con los
valores promedio para energías características de tipo iónico y
de enlace covalente (~400 kJ por mol).
Estas son ligeramente direccionales, es decir, al elevarse la temperatura,
el movimiento transicional, rotacional y vibracional de las moléculas aumenta y
produce orientación más aleatoria entre ellas. En consecuencia, la fuerza de
las interacciones dipolo-dipolo disminuye al aumentar la temperatura.
Tipos de enlace dipolo-dipolo
Los enlaces
entre dipolos permanentes ocurren
entre moléculas que tienen un momento dipolar intrínseco; esto habitualmente se
puede relacionar con una diferencia de electronegatividad. Por otro lado, los átomos y las moléculas
apolares, que no tienen un momento dipolar permanente, son polarizables,
esto es, pueden formar dipolos eléctricos como reacción a un campo eléctrico cercano. El enlace entre un átomo o
molécula apolar y una molécula dipolar se denomina dipolo permanente-dipolo inducido,
y es de alcance aún más corto.
INTERACCIONES
PUENTES DE HIDROGENO…
LOS
PUENTES DE HIDROGENO
El puente de hidrógeno es un enlace que se establece entre moléculas
capaces de generar cargas parciales. El agua, es la sustancia en donde los
puentes de hidrógeno son más efectivos, en su molécula, los electrones que
intervienen en sus enlaces, están más cerca del oxígeno que de los hidrógenos y
por esto se generan dos cargas parciales negativas en el extremo donde está el
oxígeno y dos cargas parciales positivas en el extremo donde se
encuentran los hidrógenos. La presencia de cargas parciales positivas y
negativas hace que las moléculas de agua se comporten como imanes en los que
las partes con carga parcial positiva atraen a las partes con cargas parciales
negativas. De tal suerte que una sola molécula de agua puede unirse a
otras 4 moléculas de agua a través de 4 puentes de hidrógeno. Esta
característica es la que hace al agua un líquido muy especial.
PUENTES
DE HIDROGENO DE AGUA
Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados
entre átomos electronegativos. Cuando un átomo de Hidrógeno está unido covalentemente,
a una átomo electronegativo, ej. Oxígeno o Nitrógeno,
asume una densidad (d) de carga positiva, debido a la elevada electronegatividad del átomo
vecino. Esta deficiencia parcial en electrones, hace a los átomos de Hidrógeno
susceptibles de atracción por los electrones no compartidos en los átomos de
Oxígeno o Nitrógeno
Obsérvese la configuración electrónica del Oxígeno:
8O 1s2 2s2 2pxêé pyé pzé
de ahí que :
:
 :
:
d+ d+
d-
d+ d+
d-

Enlace
por puente de hidrógeno…
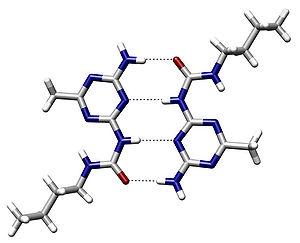
Ejemplo de enlace de hidrógeno intermolecular en un complejo dimérico autoensamblado
molecular reportado
por Meijer y colaboradores.1
Enlace de hidrógeno intramolecular en la acetilacetona,
que ayuda a estabilizar el tautómero enol
ENLACE POR PUENTE DE
HIDROGENO…
Un enlace por puente de hidrógeno o enlace
de hidrógeno es la fuerza
atractiva entre un átomo electronegativo y un átomo de hidrógeno unido covalentemente a
otro átomo electronegativo. Resulta de la formación de una fuerza dipolo-dipolo con un átomo de hidrógeno unido a un
átomo de nitrógeno, oxígeno o flúor (de ahí el nombre de "enlace de
hidrógeno", que no debe confundirse con un enlace a átomos de hidrógeno). La energía de
un enlace de hidrógeno (típicamente de 5 a 30 kJ/mol) es comparable a la de los
enlaces covalentes débiles (155 kJ/mol), y un enlace covalente típico es sólo
20 veces más fuerte que
un enlace de hidrógeno intermolecular. Estos enlaces pueden ocurrir entre
moléculas (intermolecularidad), o entre diferentes partes de una misma
molécula (intramolecularidad).2 El
enlace de hidrógeno es una fuerza de van der Waals dipolo-dipolo fija muy fuerte, pero
más débil que el enlace covalente o
el enlace iónico. El enlace de hidrógeno está en algún
lugar intermedio entre un enlace covalente y
una simple atracciónelectrostática intermolecular. Este tipo de enlace ocurre tanto en moléculas
inorgánicas tales como el agua,
y en orgánicas como el ADN.
El enlace de
hidrógeno intermolecular es responsable del punto de ebullición alto del agua (100°C). Esto es debido al fuerte
enlace de hidrógeno, en contraste a los otros hidruros de calcógenos. El enlace de hidrógeno intramolecular es
responsable parcialmente de la estructura, estructura terciaria y estructura cuaternaria de las proteínas y ácidos nucleicos.

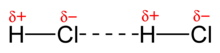
No hay comentarios:
Publicar un comentario